Dacă lucrați în Pharma, știți cât timp și bani merg în dezvoltarea de droguri. Ultimul lucru pe care îl doriți este o respingere dureroasă a FDA, una care nu numai că costă milioane de companii, dar întârzie tratamentele critice pentru pacienții care au nevoie de ei.
Respingerile de reglementare se pot întâmpla din mai multe motive, cum ar fi dovezi clinice insuficiente, preocupări de fabricație și calitate, aplicații incomplete sau date lipsă și probleme generale de siguranță. Cu toate acestea, în ultimii ani, Calitate slabă a software -ului a devenit un factor în creștere, dar adesea trecut cu vederea.
Prin „software”, ne referim nu doar la aplicații, ci și la medii de programare, limbaje și instrumente utilizate pentru procesarea și guvernarea datelor clinice. Pe măsură ce mai multe companii farmaceutice explorează tehnologii open-source precum R alături de SAS pentru analiza studiilor clinice, organismele de reglementare acordă o atenție mai atentă calității și conformității software-ului.
Având în vedere acest lucru, conformitatea GXP în dezvoltarea software -ului este esențială pentru a face această tranziție lină și sigură. În acest articol, vom examina cazurile în care problemele de calitate a software -ului au dus la respingeri costisitoare ale FDA – astfel încât să puteți afla ce să urmăriți și cum să evitați întârzieri similare.
Validarea GXP în dezvoltarea software începe cu definiția Done. Citiți modul în care Appsilon îl implementează pentru companiile Fortune 500.
Cuprins
- Problemele de calitate a software -ului sunt un motiv comun pentru respingerile FDA?
- Modul în care respingerea FDA poate costa compania dvs. trei sferturi din evaluarea acesteia-și cum să o evitați
- Rolul lui Appsilon în conformitatea GXP
Problemele de calitate a software -ului sunt un motiv comun pentru respingerile FDA?
Există multe motive pentru care FDA ar putea respinge depunerea de droguri sau poate solicita îmbunătățiri în timpul unei inspecții.
În timp ce probleme precum dovezi clinice insuficiente, preocupări de fabricație și date lipsă sunt adesea motivele cele mai citate, calitatea software -ului joacă un rol crucial în asigurarea conformității și integrității datelor.
De exemplu, prelucrarea slabă a datelor sau analizele statistice defectuoase pot duce la dovezi clinice insuficienteunde rezultatele studiului nu reușesc să demonstreze eficacitatea din cauza erorilor în gestionarea datelor. În mod similar, probleme de conformitate în Fabricarea și controlul calității Poate apărea dacă sistemele software utilizate pentru urmărirea și raportarea nu îndeplinesc așteptările de reglementare.
Următoarele motive sunt mult mai frecvente:
- Dovezi clinice insuficiente: Lipsa de date suficiente care demonstrează eficacitatea medicamentului.
- Probleme de fabricație și calitate: Nerespectarea Practici actuale de fabricație bune (CGMP), care asigură consistența și siguranța în producția de droguri.
- Aplicații incomplete sau date lipsă: Goluri în documentație sau nerespectarea rezultatelor studiului necesare.
- Probleme de siguranță: Efectele adverse ale medicamentului care îi depășesc beneficiile potențiale.
Totuși, acest lucru nu înseamnă că FDA nu acordă atenție calității software -ului.
FDA și alte organisme de reglementare examinează îndeaproape instrumentele și metodologiile utilizate în analiza datelor, raportarea studiilor clinice și trimiterile de reglementare. De asemenea, primesc datele necesare pentru a reproduce analizele făcute de sponsor.
Dacă compania dvs. folosește limbaje de programare precum R sau Python pentru aceste sarcini, FDA poate evalua dacă scripturile și procesele de validare respectă așteptările lor.
Cum o respingere FDA poate costa compania dvs. la trei sferturi din evaluarea acesteia-și cum să o evitați
Să începem cu un caz devastator de respingere FDA care a rupt o companie peste noapte.
La sfârșitul lunii noiembrie 2024, stocul Applied Therapeutics (APLT) a scăzut după ce FDA a respins medicamentul cu boala metabolică. Și când spunem „PLUMMETED”, ne referim la asta – APLT a pierdut trei sferturi din evaluarea sa aproape instantaneu:

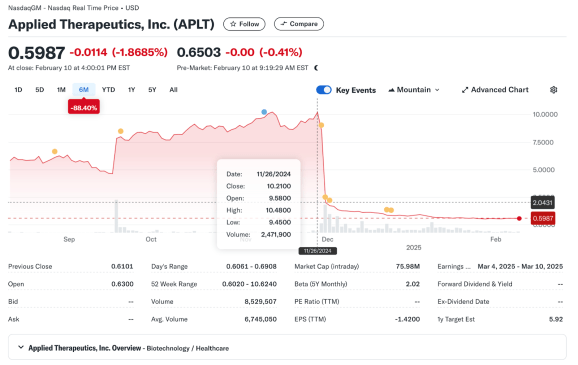
Stocul a scăzut de la un preț de închidere de 10,21 USD la 26 noiembrie la 2,03 USD pe 29 noiembrie, reprezentând o scădere de 80%.
Acum este februarie 2025, iar judecând prin grafic, compania încă nu a revenit – parțial din cauza deficiențelor evitabile în aplicația sa clinică.
Din păcate, aceasta nu este singura respingere a FDA legată de software. Iată câteva alte cazuri care evidențiază importanța GSEP (bune practici de inginerie software):
Tipuri de inspecții FDA
Dacă faceți parte dintr -o industrie extrem de reglementată, precum Pharma, sunteți probabil obișnuit cu inspecțiile FDA. Dacă nu, iată câteva motive pentru care FDA ar putea efectua o inspecție:
- Inspecții înainte de aprobare: Efectuată înainte de aprobarea unei noi cereri de medicamente pentru verificarea datelor depuse, evaluarea proceselor de fabricație și confirmarea conformității.
- Inspecții GMP de rutină: Efectuată periodic pe baza factorilor de risc, de obicei la fiecare 2 până la 4 ani.
- Inspecții pentru cauză: Declanșat de reclamații, evenimente adverse, reamintiri de produse sau rapoarte de informare.
- Inspecții de urmărire: Efectuată după o inspecție anterioară a identificat deficiențe semnificative.
- Inspecții de monitorizare a bioresearchei (BIMO): Efectuate pentru a inspecta studiile clinice, studiile de bioechivalență și practicile de laborator.
- Inspecții post-piață: Efectuată după ce un produs este pe piață pentru a asigura o calitate continuă și respectarea reglementărilor.
- Inspecții străine: Efectuate la instalații de peste mări care fabrică produse pentru piața americană.
Exemple de probleme de conformitate legate de software
Acum că cunoașteți tipurile de inspecții pe care FDA le poate efectua, să examinăm rapoartele de inspecție FDA din lumea reală care evidențiază probleme legate de software. Toate aceste rapoarte sunt disponibile public pe site -ul FDA.
Preocupările comune de FDA legate de software includ erori software, trasee de audit lipsă, defecte de securitate, lipsa proceselor de rezervă și validarea slabă a sistemelor software.
Bug -urile software găsite, iar sistemul pentru achiziția de date nu este validat în mod corespunzător:


Lipsa controalelor de securitate software, fără copii de rezervă și trasee de audit lipsă:


Fără proceduri de validare a datelor și fără controale de acces:


Software lansat fără control adecvat al schimbării:


Documentația lipsă și lipsa controlului accesului:


Lipsa controlului accesului și a validării datelor, fără trasee de audit:


Utilizarea software -ului nevalidat:

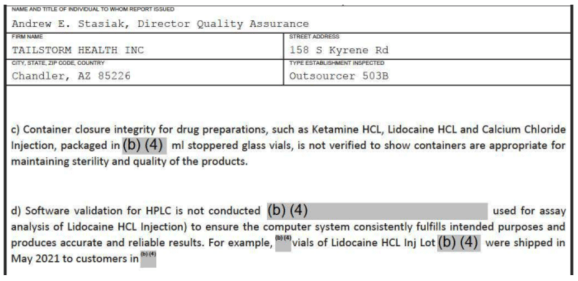
În concluzie, toate aceste exemple evidențiază GSEP insuficient (bune practici de inginerie software), ceea ce a costat probabil organizațiilor timp și bani semnificativi.
Rolul lui Appsilon în conformitatea GXP
La Appsilon, ajutăm companiile să navigheze în complexitățile conformității GXP, asigurând adoptarea rapidă a tehnologiei, în timp ce îndeplinesc cerințele de reglementare și atenuarea riscurilor de reglementare. Oferim servicii cuprinzătoare, de la Audite de conformitate GXP la construcție Tablouri de bord strălucitoare conforme În R și Python, rulând pe platforme de date scalabile și cloud.
Suntem specializați în științe farmaceutice și viață și am ajutat mai multe companii Fortune 500 să dezvolte software de înaltă calitate.
Aflați mai multe despre modul în care serviciul nostru de audit GXP vă poate ajuta să navigați pe trimiteri FDA și EMA.
În concluzie, conformitatea GXP este dificilă, în special în industrii complexe precum Pharma. În timp ce ghidul nostru cuprinzător privind navigarea conformității GXP este un loc minunat pentru a începe, nu există nicio soluție de dimensiuni.
Dacă aveți încredere în înțelegerea calității și conformității, verificați-vă de două ori disponibilitatea prin descărcarea noastră Definiția listei de verificare Done (DoD) pentru echipele farmaceutice.
Dacă aveți nevoie de un partener de încredere pentru a asigura calitatea înaltă a software -ului dvs. și a eficientiza procesul de trimitere FDA și EMA, Ajungeți la Appsilon.
Postarea a apărut mai întâi pe Appsilon.com/blog/.